プレスリリース

米国本社プレスリリース
この資料の原文は、米国エドワーズライフサイエンス社が発表した英語の報道資料です。以下の翻訳は、日本の報道機関向けに参考として提供するものです。本資料の内容・解釈については、英語版の原文を参照してください。また、文中には日本では未承認、または適応外使用となる製品についての記述が含まれることがあります。
英語版は http://www.edwards.com/newsroom/press-releases からご覧ください。
Real-Worldエビデンスがサピエン3生体弁の臨床試験成績を裏付ける
比較スタディにおいて450以上の米国の医療機関における中等度リスク症例約2,000例の結果を示す
パリ、2018年5月22日 – 構造的心疾患とクリティカルケアモニタリングに関する患者さんのためのイノベーションを世界的にリードするエドワーズライフサイエンス社(NYSE:EW)は、本日、米国の450施設を超える医療機関でのサピエン3生体弁を使用した治療において、一貫して好ましい患者アウトカムが示されることが30日データから明らかになったことを発表しました。開胸手術のリスクが中等度である重度の症候性大動脈弁狭窄症約2,000症例のデータは、少数の医療機関で実施された初期の比較臨床試験の結果と一致することが明らかになりました。
エドワーズ社経カテーテル生体弁部門担当コーポレート・バイスプレジデントのラリー・L・ウッド(Larry L. Wood)は、以下のように述べています。「多くの臨床医によって米国のReal world(臨床現場)にサピエン3生体弁が導入され、そして初期の臨床試験での優れた患者アウトカムが維持されたことを大変嬉しく思います。サピエン3弁を用いた経カテーテル大動脈弁治療はさらに多くの医療機関で実施されていることから、この手技の一般化が可能であり、また有効であることが示されています。これらの登録データは、厳密に管理された臨床試験環境から、拡大治験を経て市販後の臨床現場に移り、このような手技を必要とする患者さんに対して以前にも増して広く適用された場合でも、良好な治療成績が維持されることを示唆する重要な結果となりました」。
本日のEuroPCR 2018の最新臨床試験ホットライン セッションでは、Cleveland Clinic Abu Dhabi、Heart & Vascular Institute(心臓血管研究所)最高学術責任者兼循環器内科部長であるE. Murat Tuzcu, M.D.氏によって、PARTNER II試験の患者アウトカムと、米国胸部外科学会/米国心臓病学会(STS/ACC)経カテーテル弁治療(TVT)レジストリから収集した臨床現場におけるデータとのプロペンシティマッチング解析が発表されました。
「サピエン3弁による治療を受けた中等度リスク症例のReal worldでのアウトカムを、臨床試験の結果と比較したこれらのデータから、高い生存率および低い脳卒中発生率を含めて同程度の良好なアウトカムであることが明らかになりました」とTuzcu氏は述べました。
STS/ACC TVTレジストリに登録された中等度リスク1,956症例のアウトカムを、PARTNER II S3i試験に登録された中等度リスク652症例およびSAPIEN 3中等度リスク拡大治験(S3iCAP)に登録された652症例の術後30日のデータと比較しました。
すべての症例は経大腿アクセスで治療されました。解析における重要な臨床指標を下表に示します。
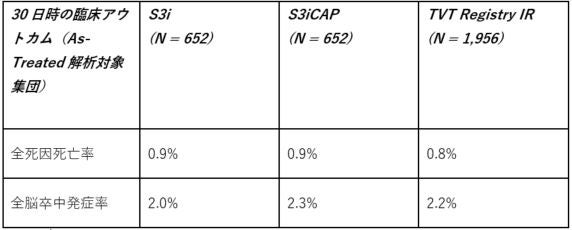
優れた生存率および脳卒中発症率に加えて、TVTレジストリにおける承認後のデータから、中等度から重度の弁周囲逆流発生率は低く、入院期間は平均2日であることが示されました。
サピエン3弁は、欧州では2014年以降、米国では2015年以降販売されています。2016年には欧州および米国の両規制当局により、中等度リスク症例向けの治療を含める適応拡大が承認されました。サピエン3弁は、数十年におよぶ生体弁開発に関する当社の経験と、SAPIEN弁の実証されたベネフィットを基盤として開発された製品です。
お問い合わせ
メディア
Amy Meshulam
(VP, Global Communications)
